河南大学淮河医院临床试验伦理委员会

一、临床试验伦理委员会审查原则
河南大学淮河医院临床试验伦理委员会作为一个独立的机构,审查以独立、客观、公正和透明为原则,遵守国家法律、法规和规章的规定和河南大学淮河医院的相关规章制度以及公认的生命伦理原则,对涉及人的生物医学研究的科学性、伦理道德进行审查,旨在为受试者提供尊严、权利、安全和福利的保证,保护受试者的权益和安全,促进社会公正。
二、临床试验伦理委员会人员组成
河南大学淮河医院伦理委员会由包括从事医药相关专业人员、非医药专业人员、法律专家,以及独立于研究/试验单位之外的人员,共11人组成,且有不同性别。
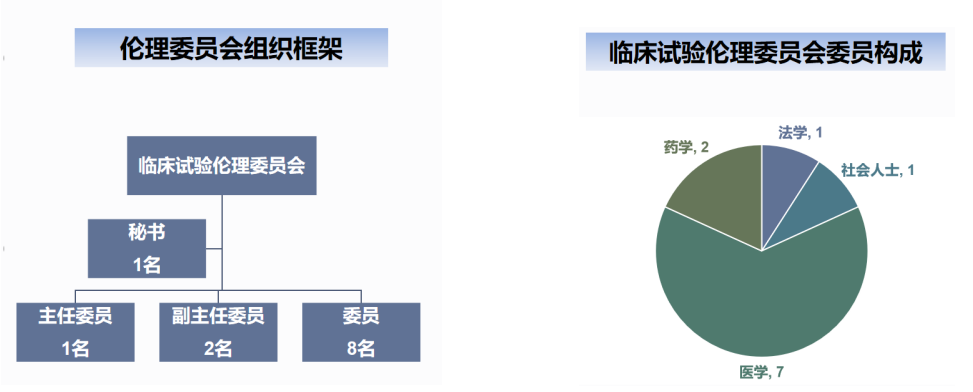
三、临床试验伦理委员会成员名单
根据工作需要,我院对临床试验伦理委员会进行了调整。新一届委员名单如下:
职务 | 姓名 | 性别 | 工作单位 | 专业 |
主任委员 | 石贞玉 | 女 | 河南大学淮河医院 | 遗传学 |
副主任委员 | 吕维玲 | 女 | 河南大学淮河医院 | 临床药学 |
副主任委员 | 汪洋 | 男 | 河南大学医学院 | 普外科 |
委员 | 张永州 | 男 | 河南大学淮河医院 | 药学/药剂科 |
委员 | 刘红林 | 男 | 河南大学淮河医院 | 神经外科 |
委员 | 贺维亚 | 女 | 河南大学淮河医院 | 神经内科 |
委员 | 陈宝平 | 女 | 河南大学淮河医院 | 肾内科 |
委员 | 傅侃达 | 男 | 河南大学淮河医院 | 普外科 |
委员 | 郑庆云 | 女 | 河南大学体育学院 | 运动人体科学 |
委员 | 陈志宽 | 男 | 河南龙文律师事务所 | 法律 |
委员 | 庞妩燕 | 女 | 河南大学淮河医院 | 内分泌科 |
四、业务范围及联系方式
河南大学淮河医院临床试验伦理委员会负责对以注册为目的的药物和医疗器械(包括诊断试剂)临床研究、上市后医疗产品评价等进行伦理审查和跟踪。
联系地址:河南省开封市西门大街115号河南大学淮河医院北院区伦理委员会办公室
联系人:侯老师
电话:0371-23906470
E-mail:hhyyllwyhbgs@163.com
五、伦理审查申请/报告要求
1.所有涉及人的研究项目,应在研究开始前提交伦理审查申请,经同意后方可实施。
2.本中心临床试验伦理委员会常规2月一次伦理会议审查,特殊情况可以紧急加会。
3.本中心伦理审查材料按照递交清单通过邮箱递交(hhyyllwyhbgs@163.com),伦理委员会办公室对递交材料进行形式审查,符合要求提交会议审查或快速审查流程。
4.会议审查意见在会后10个工作日内传达,快速审查意见在会后5个工作日内传达。
5.送审文件清单间文件下载中具体要求。
六、伦理审查相关文件下载